消息 | 华为4款产品拟纳入医疗器械优先审批程序
近日,华为终端有限公司4款医疗器械产品拟纳入广东省医疗器械优先审批程序。
广东省直通车服务重点企业可享受优先审评
根据广东省药监局发布的《广东省第二类医疗器械优先审批申请审核结果公示(第四十九期)》显示,申请人华为终端有限公司(以下简称:华为)的四款产品拟纳入广东省医疗器械优先审评程序,四款产品分别是腕部心电血压记录仪、心电分析系统、心率失常分析系统和腕部单导心电采集器。

根据《广东省食品药品监督管理局第二类医疗器械优先审批程序》规定,符合七种情形之一的广东省第二类医疗器械首次注册申请实施优先审批,这七种情形分别是(一)临床急需且在本省尚无同品种产品获准注册的医疗器械;(二)省内已有同类产品上市,但产品供应不能满足突发公共卫生事件应急处理需要的医疗器械;(三)诊断或者治疗罕见病、恶性肿瘤,且具有明显临床优势的医疗器械;(四)诊断或者治疗老年人特有和多发疾病,且目前尚无有效诊断或者治疗手段的医疗器械;(五)专用于儿童,且具有明显临床优势的医疗器械;(六)列入国家、广东省科技重大专项或者国家、广东省重点研发计划的医疗器械;(七)广东省战略性新兴产业骨干企业、广东省直通车服务重点企业等广东省重点扶持的医疗器械生产企业申请注册的医疗器械。
此次华为进入优先审批是符合第七种情形,即为广东省直通车服务重点企业申请注册的医疗器械。
华为不断推进可穿戴设备的医疗布局
近年,苹果、OPPO等科技公司都纷纷加强了可穿戴设备在医疗器械领域的布局,2020年9月,OPPO的腕部单导联心电采集器获得国家药监局II 类医疗器械注册证。今年6月,苹果的移动心电图房颤提示软件获得医疗器械注册证,成为其在中国取得的首个医疗器械注册证。
2016年,华为发布了《5G的5大行业应用方向白皮书》提出5G在医疗行业的应用,包括远程监控可穿戴医疗、远程手术、远程影像会诊、远程医疗、资产监管五大方面。
2019年3月,华为变更经营范围,新增医疗器械(第二类医疗器械)销售等业务。
2020年4月,华为再度增加经营范围,从销售医疗器械(第二类医疗器械)扩展至了开发、生产、销售医疗器械(第一类、第二类、第三类医疗器械)。值得一提的是,离开华为的荣耀终端有限公司的经营范围也包括了医疗器械开发、生产、销售。
2020年10月30日,华为发布了WATCH GT 2 PRO ECG款,这是华为首款获得国家药品监督管理局二类医疗器械注册证的智能穿戴医疗设备,标志着华为正式有医疗器械产品进入市场。
本次4款产品进入优先审批通道,一方面凸显了华为在可穿戴医疗设备领域的技术研发能力;另一方面也可以看出华为正在通过可穿戴相关产品不断强化医疗监测类产品的建设能力,进而提升其自身可穿戴设备的市场竞争力。
政策引导可穿戴设备的数字医疗发展
近年来,国家相继发布《关于促进“互联网﹢医疗健康”发展的指导意见》、《关于深入开展“互联网﹢医疗健康”便民惠民活动的通知》、《关于完善“互联网﹢”医疗服务价格和医保支付政策的指导意见》等重要文件,支持和鼓励“互联网﹢医疗”等新服务模式的探索与发展。同时,全国多地也在积极加强相关工作引导。
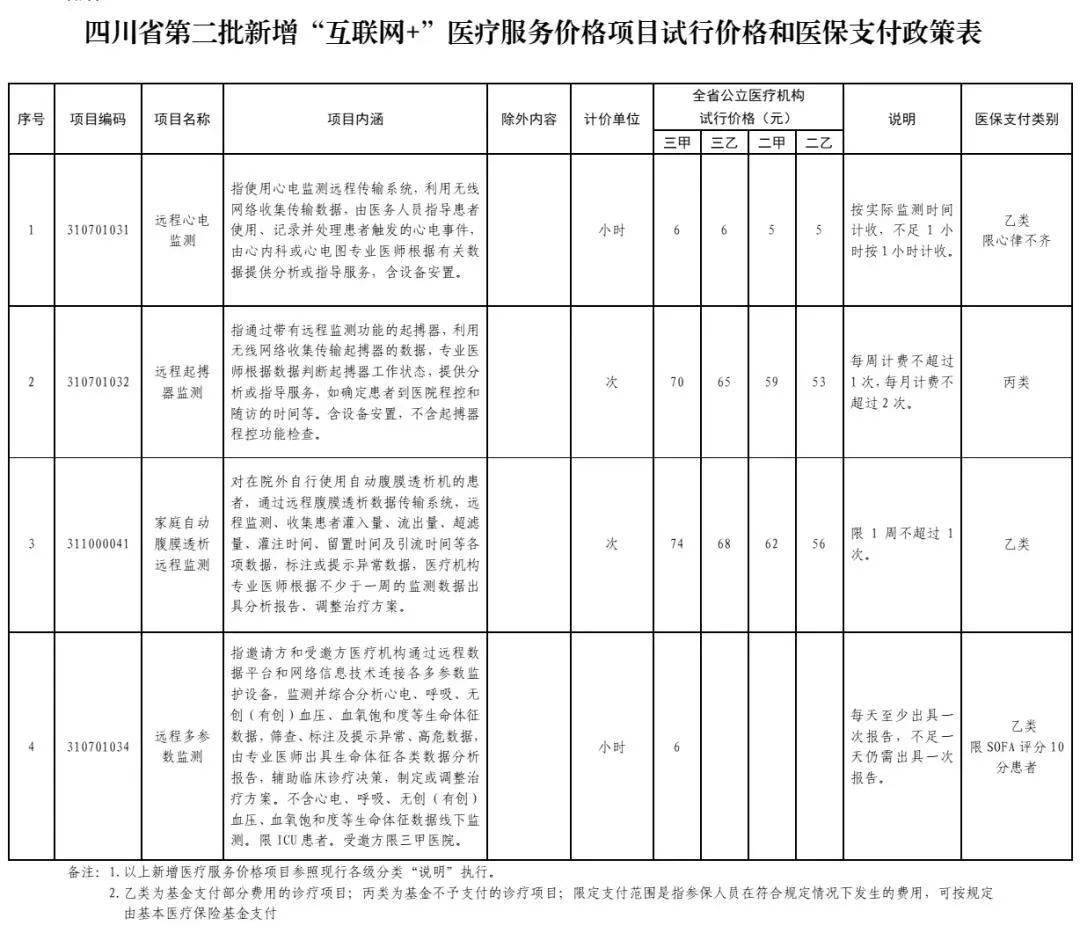
2021年7月,四川省医保局发布《互联网+医疗服务价格项目试行价格和医保支付政策专家论证结果的公示》。公示新增4项互联网+医疗服务价格项目,其中远程心电监测根据支付标准纳入医保乙类支付。医谷分析认为,一定程度上在引导具有远程监测产品的发展。
虽然目前华为、OPPO 等拿到国家医疗器械注册证的产品仅限于数据的记录和回放,不具备分析和诊断功能,但从其不断加强相关功能的布局以及基于其巨大的市场产品基数,伴随着互联网+医疗和科技技术的不断成熟,医谷认为其必然会逐步探索医疗收费的可能,拓展其产品增值服务的收益。